반응형

01 이론산소량과 이론공기량
1. 이론 산소량(Oo)
어떤 연료를 이론적으로 완전연소시키는데 필요한 산소량을 말함
가연성분인 C,H,S 이 연소할 때 필요로 하는 산소량의 합



※ 기체연료의 이론연소 양론식

2. 이론 공기량(Ao)
연료가 소비한 산소량은 공기 중에 있는 산소를 소비한 것이기 때문에 공기의 소비량으로 환산한 값
| 중량조성(%) | 체적조성(%) | ||
| 공기 1몰 중 | 질소(N₂) | 76.8 | 79 |
| 산소(O₂) | 23.2 | 21 |


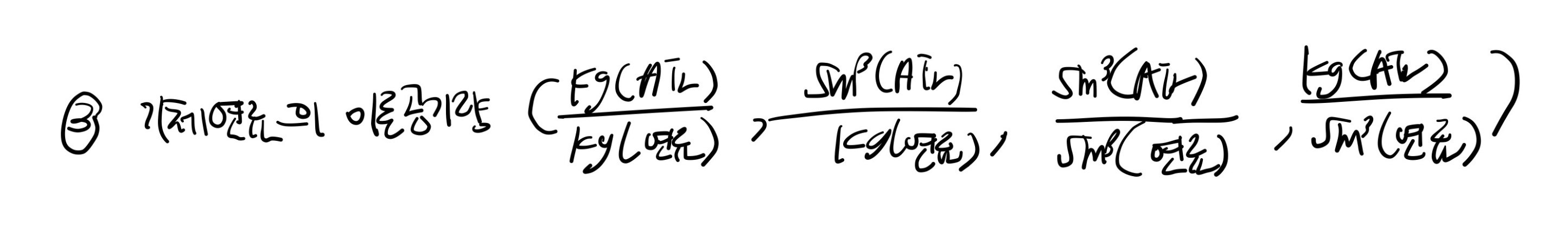
02 이론가스량과 실제가스량, 공기비
1. 이론가스량(Go)
이론가스량 = 배출가스량 = 연소시 사용한 이론공기 중 질소량 + 모든 생성물의 총합
건조생성물의 의미는 수분(H₂)을 제외한 나머지 생성물의 합

2. 실제공기(A)와 공기비(m)
1) 실제공기
실제 연소과정에서 필요로 하는 공기량으로 이론공기량보다 많은 과잉공기를 공급
실제공기(A) = 공기비 (m) X 이론공기(Ao)
실제공기(A) = 이론공기(Ao) + 과잉공기
과잉공기 = m X Ao -Ao = (m-1)Ao
2) 공기비, 과잉공기계수(m) (m≥1)
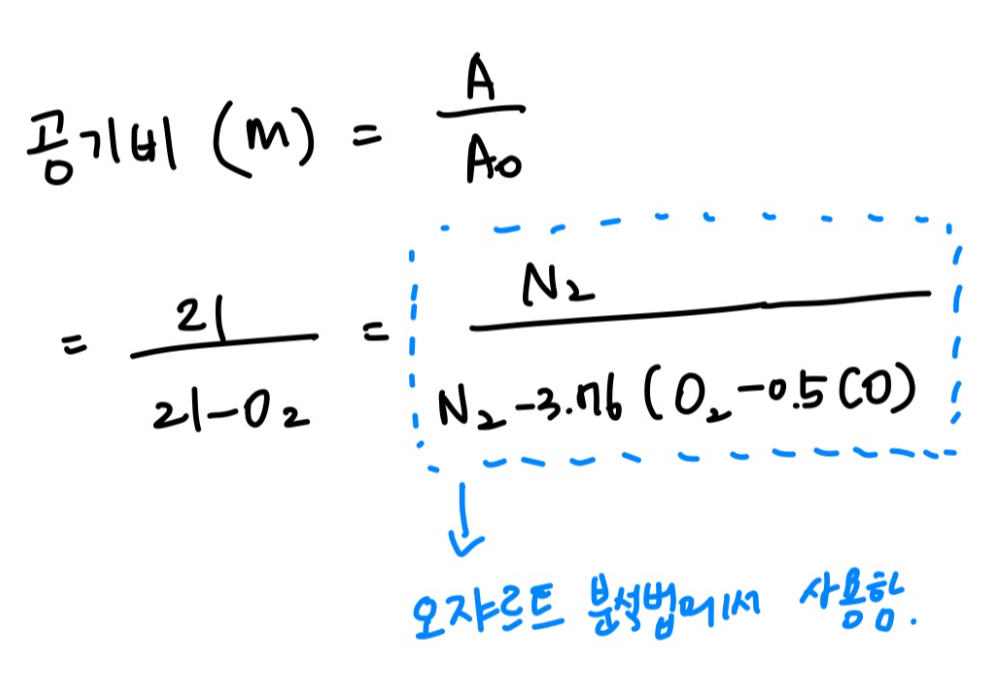
☆공기비가 연소에 미치는 영향
| 공기비가 너무 큰 경우 | 공기비가 너무 작은 경우 |
| 연소실 내의 온도저하 | 불완전연소로 매연 발생 |
| 통풍력이 강해져 배가스에 의한 열손실 증가 | 연소효율 저하 |
| 배기가스 중 NOx, SOx 증가에 의한 부식 | CO에 의한 폭발 위험 |
3) 실제가스량(G)
실제가스량 = 이론가스량 + 과잉공기량
과잉공기량 = (m-1)Ao
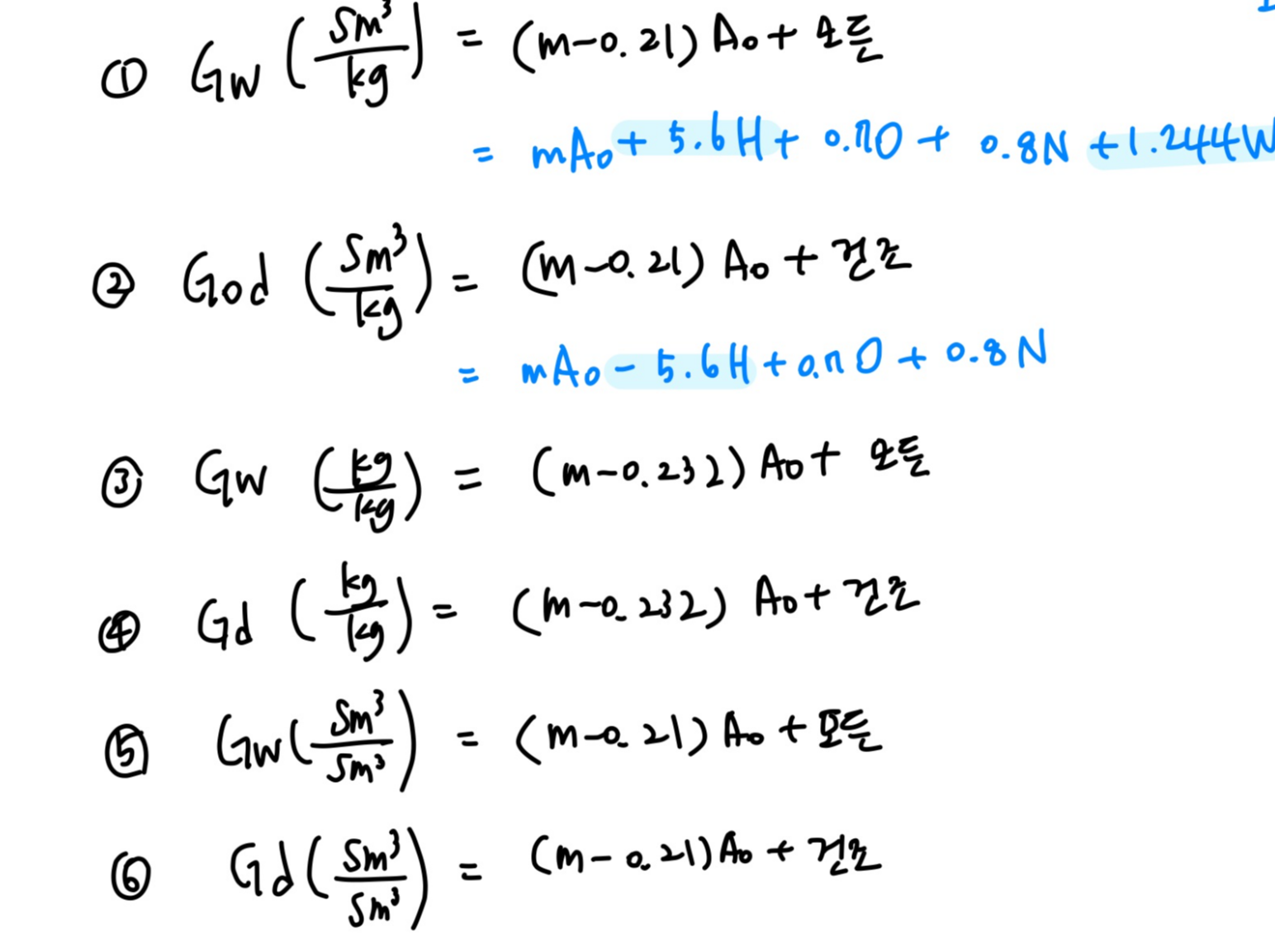
03 최대탄산가스율(CO₂max%)와 배출가스량의 성분(% , ppm) 계산
1. 최대탄산가스율(CO₂max %)
1) 연료의 성분조성(%)으로 계산하는 법
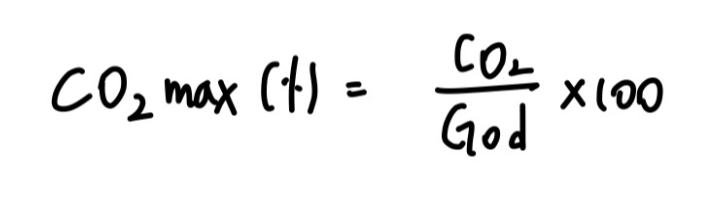
2) 배출가스 조성(%)으로 계산하는 법
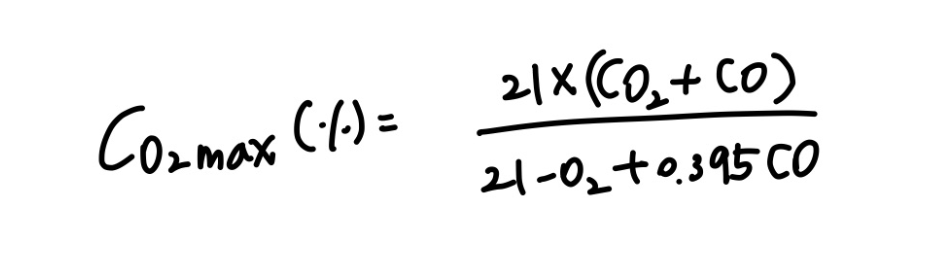
2. 배출가스 중의 포함된 성분(%, ppm)
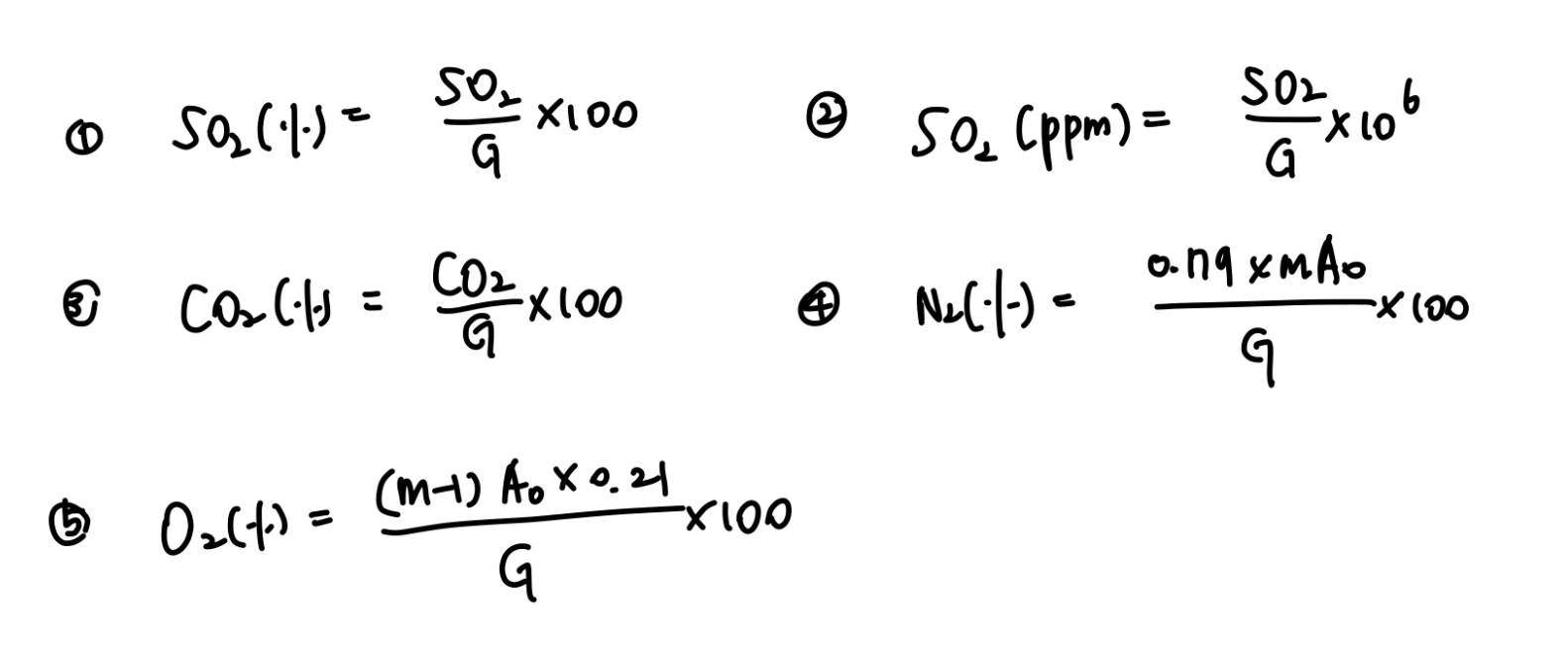
※ 여기서 , G : 가스량(S㎥)으로서 모든 가스량(Gow, God, Gw, Gd)으로 표현가능하기 때문에 반드시 문제의 조건에서 찾아야함.
'대기환경기사 > 대기환경기사 1,2,3단원' 카테고리의 다른 글
| [2. 연소공학] 05 화학반응속도 방정식 (0) | 2023.02.09 |
|---|---|
| [2. 연소공학] 04 등가비와 연소열화학 (0) | 2023.02.09 |
| [2. 연소공학] 02 연소장치의 종류와 특징 (0) | 2023.02.05 |
| [2. 연소공학] 01 연소이론 (0) | 2023.02.05 |
| [1. 대기오염개론] 08 대기오염사건 (0) | 2023.01.29 |




댓글